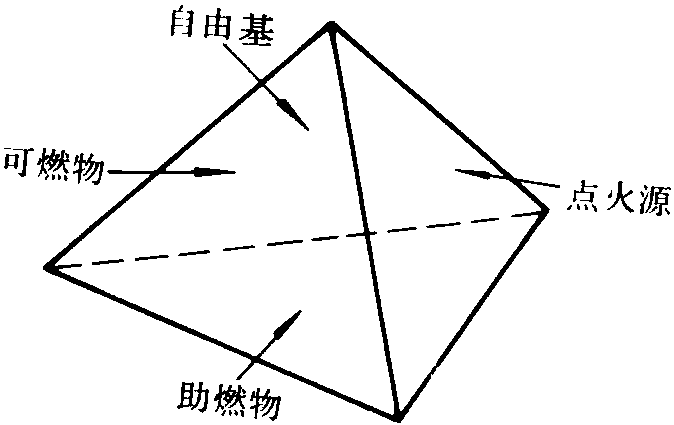
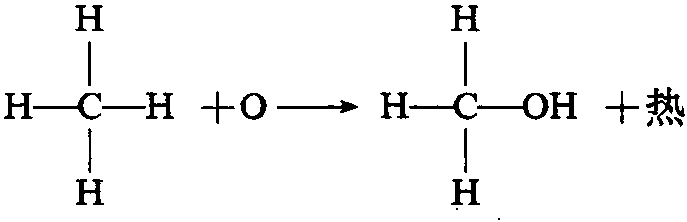连锁反应
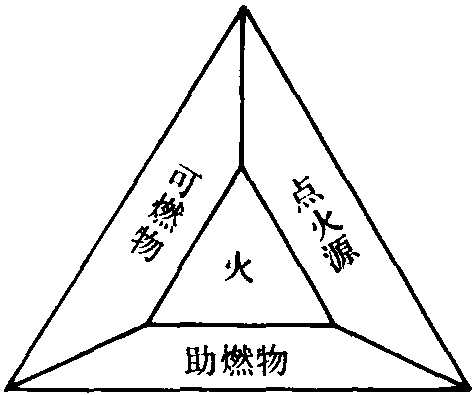
又称链式反应。当一个分子被活化后,引起许多分子都能连续不断地进行的化学反应。即瞬间进行的游离基循环链式反应,在现代科学技术中用以解释物质燃烧的机理。在本来反应进行缓慢的某些化合物中,引入或设法使之产生少量的活化中心(即游离基),可使其发生连锁反应。在某些情况下,如加入抑制剂,活化中心就会消失,连锁反应就会中断,从而使化学反应停止。例如,氢与氯混合物在光照射下,氯分子吸收光能而分解为活化原子,使混合物发生连锁反应而爆炸: Cl2Cl+Cl; Cl+H2→HCl+H;H +Cl2→HCl+Cl等等。在把链式反应的理论应用于某些物质氧化过程的理论研究时,称为氧化链式理论。这个理论 ...... (共379字) [阅读本文]>>

 上一篇
上一篇